Ex-Rad - Википедия - Ex-Rad
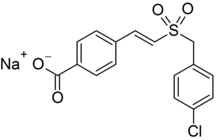 | |
| Имена | |
|---|---|
| Название ИЮПАК Натрий 4 - [(E) -2 - [(4-хлорфенил) метилсульфонил] этенил] бензоат | |
| Идентификаторы | |
3D модель (JSmol ) | |
| КЕГГ | |
PubChem CID | |
| UNII | |
| |
| Характеристики | |
| C16ЧАС12ClNaО4S | |
| Молярная масса | 358.77 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Экс-рад (или же Бывший RAD; рецилисиб натрия (ГОСТИНИЦА, USAN ); код разработки ON 01210.Na) является экспериментальным наркотиком. развитый компании Onconova Therapeutics и Министерство обороны США.[1] Он изучается как средство радиационной защиты.[2] Химически это натриевая соль 4-карбоксистирил-4-хлорбензилсульфона.[3]
Клинические испытания
Результаты двух Фаза I Клинические исследования на здоровых добровольцах показывают, что подкожно вводимый Ex-Rad безопасен и хорошо переносится, «без признаков системных побочных эффектов».[4] Исследование на мышах продемонстрировало эффективность Ex-Rad за счет увеличения выживаемости мышей, подвергшихся обычно смертельному облучению всего тела. В исследовании тестировались устные и парентеральный применение Ex-Rad как для пред-, так и для постэкспозиционной радиопомощи.[1]
Исследования Ex-Rad проводились в сотрудничестве с Научно-исследовательский институт радиобиологии Вооруженных Сил (AFRRI), кафедра биохимии, молекулярной и клеточной биологии Джорджтаунский университет, Университет Лонг-Айленда фармацевтического колледжа Арнольда и Мари Шварц и кафедры онкологических наук Mt. Синайская медицинская школа.[1]
Механизм действия
Онконова сообщает, что Ex-Rad защищает клетки, подвергшиеся облучению, от повреждения ДНК, и что механизм действия препарата не включает удаление свободные радикалы или арест клеточный цикл. Вместо этого они утверждают, что в нем используется «новый механизм», включающий «внутриклеточную передачу сигналов, обнаружение повреждений и пути восстановления ДНК».[4] Ex-RAD - это производное хлорбензилсульфона, которое действует после того, как свободные радикалы повредили ДНК. Генеральный директор Onconova Рамеш Кумар считает, что это лучший подход, чем попытки избавиться от свободных радикалов. «Свободные радикалы очень недолговечны, поэтому окно возможностей для введения лекарства очень узкое», - говорит он. В моделях клеток и животных Ex-RAD защищает кроветворный и желудочно-кишечный ткани от радиационного поражения при введении до или после облучения.[5]
Смотрите также
- Энтолимод
- CBLB502 соединение, которое изучается на его способность подавлять апоптотический смерть клетки в кроветворный и желудочно-кишечный клетки.[5]
- Амифостин (WR2721), первый селективный радиопротектор с широким спектром действия, активирует Ремонт ДНК[6]
- Филграстим (Neupogen), кроветворное средство противодействия острый лучевой синдром (ARS)
- Пегфилграстим (Neulasta), действует дольше, чем его родитель, филграстим
- Сарграмостим (лейкин), аналогичный по применению филграстим
- N-Ацетилцистеин, защищает от повреждения ДНК, считается сопоставимым с амифостином[7][8][9][10]
- Тромбомодулин[11]
- Активированный протеин C[11]
- Хелаторная терапия, средство противодействия внутренним радиоизотоп загрязнение
- DPTA, хелатирующий агент, используемый для устранения актиниды которые были проглочены, один из трех Управление по контролю за продуктами и лекарствами (FDA) запасы радиозащитных средств[5]
- Берлинская лазурь /радиогардаза, хелатирующий агент для лечения радиоактивныхЦезий и таллий потребление, одно из трех хранимых FDA радиозащитных средств[5]
- Йодистый калий, а профилактический препарат рекомендуется перед введением радиоактивный йод окружающей среде, один из трех запасов радиозащиты FDA[5]
- Койевая кислота
- Гиалуронан
- Эффект Петкау
Рекомендации
- ^ а б c «Onconova Therapeutics представляет новые данные, демонстрирующие радиозащиту с помощью Ex-RAD, на ежегодном собрании RRS» (Пресс-релиз). EurekAlert. 27 сентября 2010 г. Архивировано из оригинал на 2011-03-22. Получено 2011-03-22.
- ^ «Рецилисиб». Adis Insight.
- ^ Ghosh, Sanchita P .; Перкинс, Майкл У .; Хибер, Кевин; Кулкарни, Шилпа; Као, Цзы-Чег; Редди, Э. Премкумар; Редди, М. В. Рамана; Maniar, Manoj; Сид, Томас; Кумар, К. Шри (2009). «Радиационная защита с помощью нового химического вещества, Ex-Rad: эффективность и механизмы». Радиационные исследования. 171 (2): 173–9. Bibcode:2009РадР..171..173Г. Дои:10.1667 / RR1367.1. PMID 19267542.
- ^ а б «Ex-RAD® для защиты от радиационных повреждений». Онконова терапия. 2009. Архивировано с оригинал на 2011-03-22. Получено 2011-03-22.
- ^ а б c d е «Наркотики, которые нельзя использовать». Новости химии и машиностроения. 90 (26): 23–26. 2012.
- ^ Kouvaris, J. R .; Кулулиас, В. Э .; Влахос, Л. Дж. (2007). «Амифостин: первый селективный радиопротектор широкого спектра действия». Онколог. 12 (6): 738–47. Дои:10.1634 / теонколог. 12-6-738. PMID 17602063.
- ^ Релиене, Рамуне; Поллард, Джулианна М .; Соболь, Жанна; Труйлер, Бенедикт; Гатти, Ричард А .; Шистл, Роберт Х. (2009). «N-ацетилцистеин защищает от повреждения ДНК, вызванного ионизирующим излучением, но не от гибели клеток у дрожжей и млекопитающих». Мутационные исследования / Фундаментальные и молекулярные механизмы мутагенеза. 665 (1–2): 37–43. Дои:10.1016 / j.mrfmmm.2009.02.016. PMID 19427509.
- ^ Mansour, Heba H .; Hafez, Hafez F .; Фахми, Надя М .; Ханафи, Немат (2008). «Защитный эффект N-ацетилцистеина против радиационного повреждения ДНК и гепатотоксичности у крыс». Биохимическая фармакология. 75 (3): 773–80. Дои:10.1016 / j.bcp.2007.09.018. PMID 18028880.
- ^ Демирель, К; Kilçiksiz, S; Да, О.И. Gürgül, S; Да, я; Эрдал, Н. (2009). «Влияние N-ацетилцистеина на радиационно-индуцированную генотоксичность и цитотоксичность в костном мозге крыс». Журнал радиационных исследований. 50 (1): 43–50. Bibcode:2009JRadR..50 ... 43D. Дои:10.1269 / младший.08066. PMID 19218780.
- ^ Демирель, К; Кильциксиз, С; Evirgen-Ayhan, S; Гургуль, С; Эрдал, Н. (2010). «Профилактический эффект N-ацетилцистеина на радиационный дерматит на модели крыс». Журнал Балканского союза онкологов. 15 (3): 577–82. PMID 20941831.
- ^ а б Гейгер, Хартмут; Pawar, Snehalata A; Кершен, Эдвард Дж; Наттамаи, Калпана Дж; Эрнандес, Ирэн; Лян, Хай По Х; Фернандес, Хосе Б; Канселас, Хосе А; Райан, Марни А; Кустикова Ольга; Шамбах, Аксель; Фу, Цян; Ван, Джунру; Финк, Луи М; Петерсен, Карл-Уве; Чжоу, Даохун; Гриффин, Джон Х; Баум, Кристофер; Вейлер, Хартмут; Хауэр-Йенсен, Мартин (2012). «Фармакологическое нацеливание на путь активированного тромбомодулином протеина С снижает радиационную токсичность». Природа Медицина. 18 (7): 1123–9. Дои:10,1038 / нм 2813. ЧВК 3491776. PMID 22729286.
